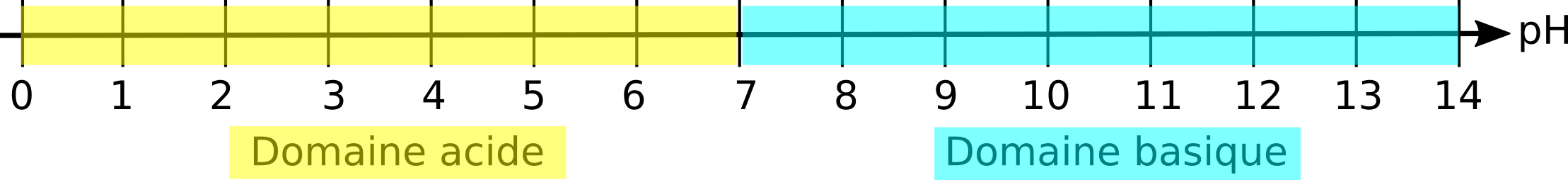
■ Les ions H+ sont les ions responsables du caractère acide d'un milieu. L'acidité d'une solution aqueuse est quantifiée par son potentiel d'hydrogène, noté pH. C'est une grandeur sans unité et sans dimension. Sa valeur dans les solutions aqueuses est comprise entre 0 et 14. Si le pH d'une solution est compris entre 0 et 7, la solution est acide. S'il vaut 7, elle est neutre. S'il est supérieur à 7, elle est basique. Plus la solution est concentrée en ions H+, plus son pH est petit. Le pH peut être mesuré à l'aide d'un pH-mètre, ou bien il peut être plus simplement estimé à l'aide d'un papier pH : au contact d'une solution, le papier prend une couleur qui révèle la valeur du pH.
■ L'hydrogène est le plus simple élément chimique. Occupant la première case du tableau périodique, son noyau n'est composé que d'un seul proton. L'atome, électriquement neutre, s'entoure donc d'un unique électron. Si cet unique électron est cédé au cours d'une transformation d'oxydation de l'atome, il se forme l'ion H+, composé alors d'un simple proton.
■ La concentration d'un soluté en solution peut être quantifiée à l'aide de deux grandeurs :
- la concentration en masse de soluté dans la solution, c'est la masse de soluté par unité de volume de solution. Elle est souvent exprimée en g·L-1 ;
- la concentration en quantité de matière de soluté dans la solution, c'est la quantité de matière de soluté par unité de volume de solution. Elle est souvent exprimée en mol·L-1.