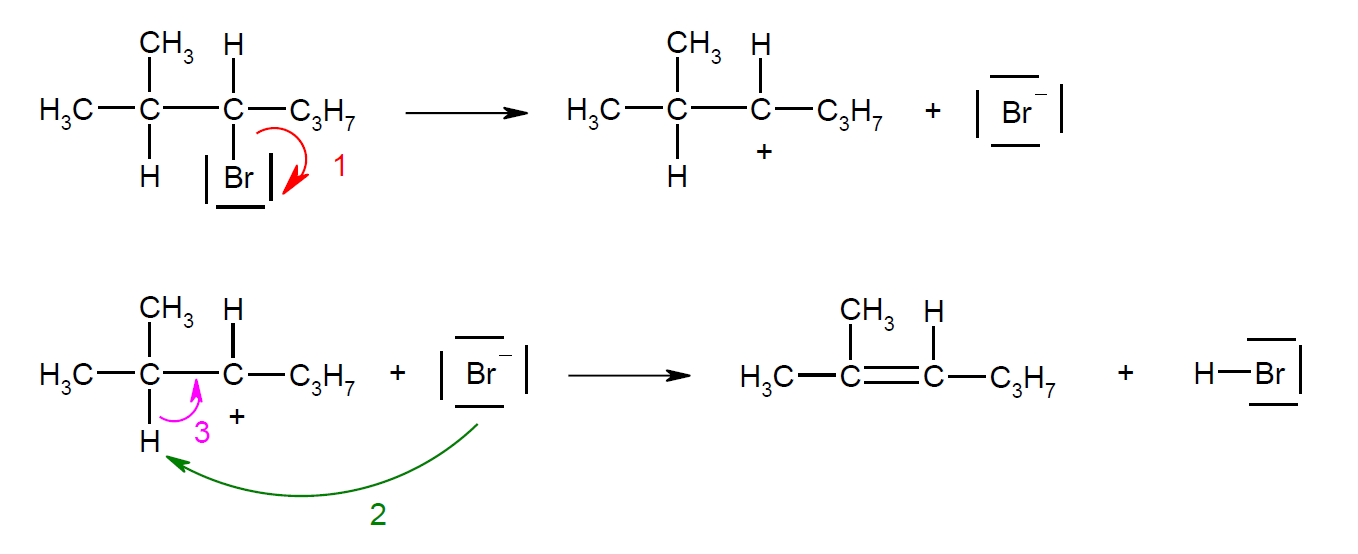
■ Une liaison covalente est formée entre deux atomes par la mise en commun de deux électrons de valence. Former une liaison libère de l'énergie, ce qui stabilise l'édifice. En revanche, briser une liaison consomme de l'énergie.
■ Si un atome n'engage pas tous ses électrons de valence dans la formation de liaisons covalentes avec d'autres atomes, les électrons de valence en surnombre se disposent par deux au voisinage de l'atome et forment un doublet non-liant. Les doublets non-liants participent, entre autres, à expliquer la géométrie des entités chimiques en raisonnant par répulsion des paires électroniques.
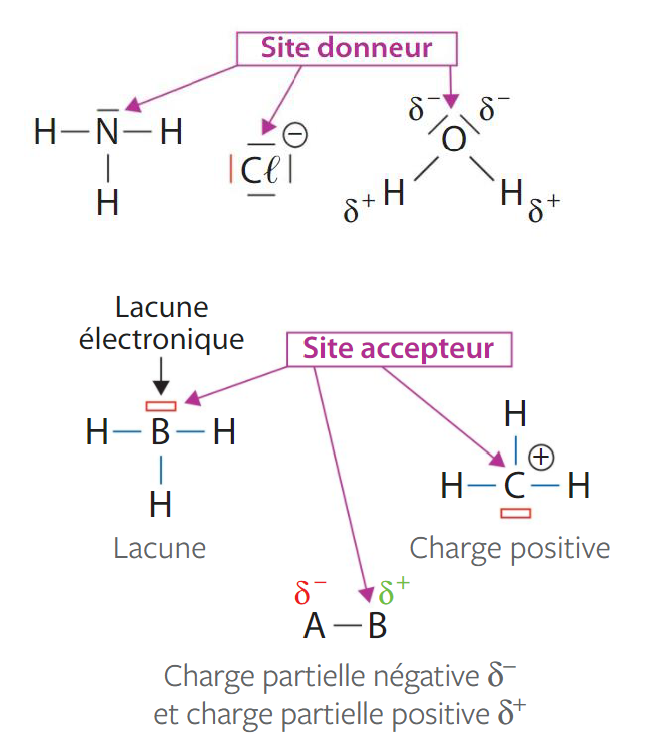
■ L'électronégativité d'un élément chimique désigne la tendance d'un atome de cet élément à attirer vers lui les électrons des liaisons covalentes qu'il engage. Une liaison formée entre deux atomes est polarisée si ces deux atomes n'ont pas la même électronégativité. Le plus électronégatif des deux s'entourent d'un nuage électronique plus dense, ce qui se modélise par une charge partielle négative notée δ-. Par appauvrissement en électron, l'autre atome est porteur d'une charge partielle positive δ+.
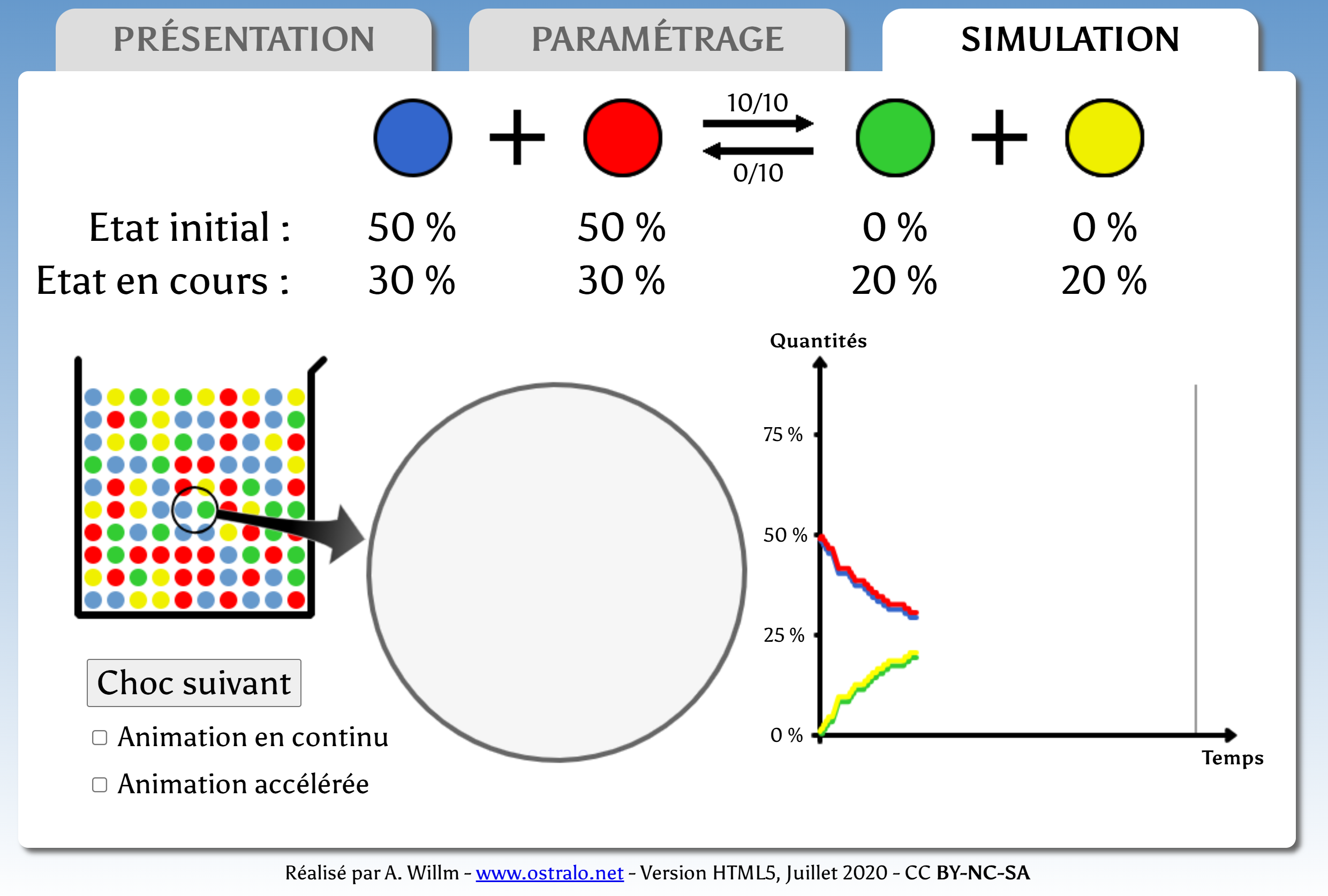
■ La température d'un système est la mesure macroscopique de l'agitation des particules à l'échelle microscopique. Plus la température est grande, plus les particules s'agitent.