Réaction d'autoprotolyse de l'eau
Notre étude s'intéresse d'abord à l'eau, parce qu'elle est le solvant de toutes nos solutions et parce qu'elle est conjuguée
aux ions oxonium qui permettent de mesurer le pH des solutions.
Puisque l'eau est une espèce amphotère, une molécule d'eau peut se comporter comme un acide en face d'une molécule d'eau qui
se comporte comme une base. Il se produit donc un transfert d'ion `H^+` entre deux molécules d'eau. On parle de la
réaction d'autoprotolyse de l'eau.
Demi-équation de déprotonation de l'eau :
`H_2O(ℓ)=HO^(-) (aq) + H^+`
Démi-équation de protonation de l'eau :
`H_2O(ℓ)+H^+=H_3O^+ (aq)`
Équation de la réaction d'autoprotolyse :
`2 H_2O(ℓ) ⇌ H_3O^+ (aq)+HO^(-) (aq)`
Une fois l'état d'équilibre atteint, les concentrations en ions oxonium et en ions hydroxyde ne sont pas indépendantes,
elle vérifie l'égalité suivante qui définit le produit ionique de l'eau :
`K_e={[H_3O^+(aq)]_"éq"\cdot[HO^(-)(aq)]_"éq"}/{c°^2}`
À 25 °C, le produit ionique de l'eau vaut en toutes circonstances `K_e=1\times10^-14`.
Remarque : dans la suite de l'étude, pour simplifier la lecture, il arrivera que les notations (aq) et éq
ne figurent plus. Il faudra les lire implicitement.
Comme cela a été fait dans la définition de pH, nous réemployons l'opérateur p pour définir le pKe :
`pKe=-log(Ke)=14` à 25 °C
Acides faibles et acides forts
Parmi tous les acides disponibles dans la nature, deux catégories sont identifiables : les acides faibles
et les acides forts. Dans la suite de notre étude, pour désigner un acide quelconque, nous emploierons
la notation `AH`, dont la base conjuguée sera notée `A^(-)`.
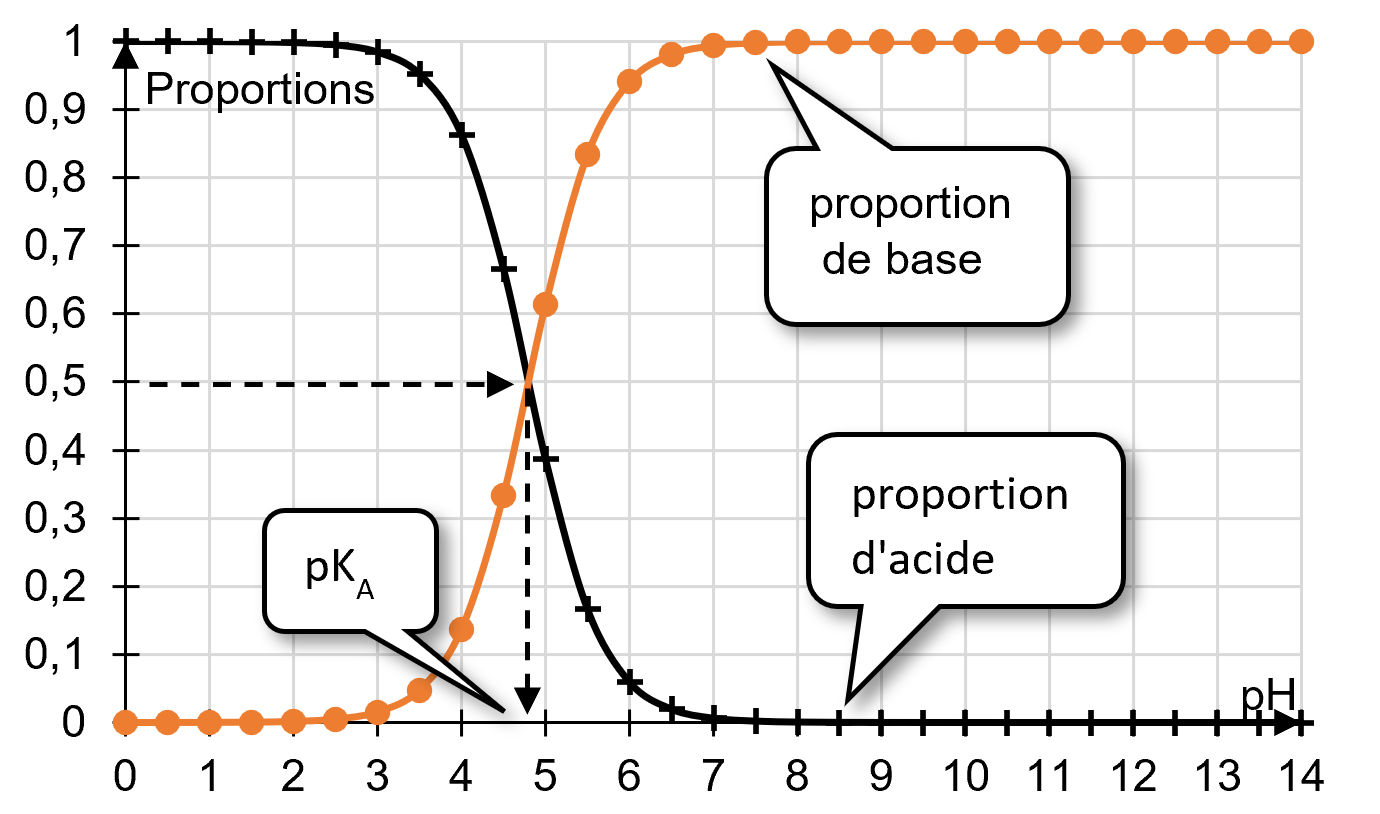
Un acide est faible si sa réaction avec l'eau est limitée. L'eau joue
alors le rôle de base, il se forme son acide conjugué. Ainsi, l'équation de la réaction s'écrit :
`AH(aq)+H_2O(ℓ) ⇌ A^(-)(aq)+H_3O^+(aq)`
Puisque la réaction est limitée, `x_f < x_"max"` et le taux d'avancement final `\tau_f < 1`.
La plupart des acides sont faibles, c'est notamment le cas des suivants :
- les acides carboxyliques comme l'acide éthanoïque, l'acide butanoïque, etc. ;
- l'acide carbonique (dioxyde de carbone dissous dans l'eau) `CO_2, H_2O` ;
- l'acide hypochloreux (dans l'eau de Javel), de formule `HCℓO` ;
- l'acide cyanhydrique (conjugué de l'ion cyanure), de formule `HCN` ;
- etc.
Inversement, un acide est fort si sa réaction avec l'eau est totale. Alors :
`AH(aq)+H_2O(ℓ) \to A^(-)(aq)+H_3O^+(aq)`
À la fin de la transformation, il ne reste plus du tout d'acide en présence, il a été totalement
consommé. Le taux d'avancement final vaut 1. Puisque la stoechiométrie est de 1 pour 1, toute la quantité
de matière en acide consommée est égale à la quantité de matière en ion oxonium formé.
Si la concentration en acide apporté est notée `c`, alors le pH à la fin de la transformation vérifie :
`pH=-log(c/{c°})`
Parmi les acides forts figurent
- l'acide chlorhydrique, de formule `H_3O^+(aq), Cℓ^(-)(aq)` ;
- l'acide sulfurique, de formule `H_2SO_4` ;
- l'acide nitrique, de formule `HNO_3` ;
- etc.
Exemple d'une solution d'acide chlorhydrique de concentration égale à 0,10 mol/L :
`pH=-log(c)=-log({0,10}/1)=1`
Bases faibles et bases fortes
Nous noterons `B` la formule d'une base et `BH^+` celle de son acide conjugué.
Une base est faible si sa réaction avec l'eau est limitée. Ainsi,
`B(aq)+H_2O(ℓ) ⇌ BH^+(aq) + HO^(-)(aq)`
Le taux d'avancement final de la transformation est inférieur à 1.
Parmi les bases fortes figurent
- les ion carboxylates, comme l'ion éthanoate, l'ion butanoate, etc. ;
- les amines comme l'ammoniac de formule `NH_3` ;
- etc.
Inversement, une base est forte si sa réaction avec l'eau est totale. Alors
`B(aq)+H_2O(ℓ) \to BH^+(aq) + HO^(-)(aq)`
À l'état d'équilibre final, le taux d'avancement vaut 1. Toute la base a été consommée,
c'est donc la quantité d'ions hydroxyde qui a été formée. Si une base forte de concentration `c`
occupe une solution de volume `V`,
`n_(f)(HO^-)=c\cdotV`
donc en termes de concentration,
`[HO^-]_"éq"=c`
grâce au produit ionique de l'eau, nous connaissons la concentration en ions oxonium :
`[H_3O^+]_"éq"=c°^2\cdot K_e/{[HO^-]_"éq"}`
`[H_3O^+]_"éq"=K_e\cdot {c°^2}/c`
Le pH de la solution vaut donc
`pH=-log({[H_3O^+]_"éq"}/{c°})`
`pH=-log(K_e\cdot {c°}/c)`
`pH=-log(K_e)-log({c°}/c)`
donc
`pH=pK_e+log(c/{c°})`
Parmi les bases fortes figure notamment la soude, solution aqueuse d'hydroxyde de sodium, de formule
`Na^+(aq), HO^(-)(aq)`.
Ex. de soude de concentration en soluté apporté égale à `2\times10^-4 mol//L` :
`pH=14+log({2\times10^-4}/1)\approx 10,3`