■ Des méthodes physiques ont été employées en classe de Seconde pour identifier les
espèces chimiques présentes dans le système. En Première, l'interaction entre la lumière et
la matière a permis de déterminer certaines caractéristiques de la matière, c'est le principe
de la spectroscopie :
- spectroscopie UV-visible avec la loi de Beer-Lambert ;
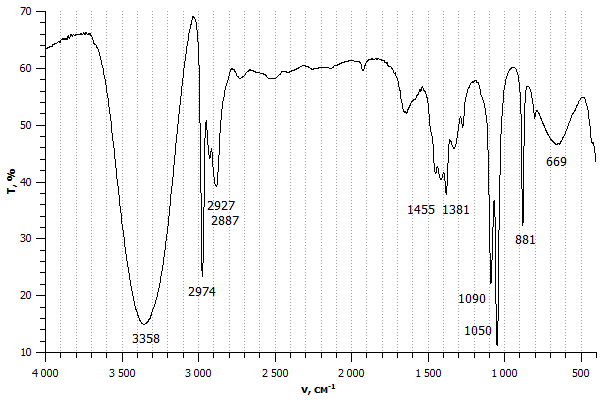
- spectroscopie IR pour l'identification des liaisons covalentes.
Le lecteur est vivement encouragé à refaire l'étude de ces deux chapitres.
■ Les molécules sont des entités chimiques électriquement neutres. Elles sont
formées par des atomes liés entre eux par des liaisons covalentes.
Les ions monoatomiques sont formés par l'ionisation d'un atome. Il se forme
un anion, porteur d'une charge électrique de signe négatif, si l'atome gagne un ou
plusieurs électrons. C'est par exemple le cas de l'ion fluorure F-.
Il se forme un cation, porteur d'une charge électrique de signe
positif, si l'atome perd un ou plusieurs électrons. C'est le cas par exemple de l'ion
sodium Na+.
Il existe également des ions polyatomiques, formés à partir de molécules et porteurs
d'une charge électrique non nulle, par exemple les ions sulfate SO42-
ou les ions ammonium NH4+.
■ Un courant électrique correspond, à l'échelle microscopique, à un flux
de charges électriques. Une molécule, étant neutre, n'y participe pas. Les ions peuvent
en revanche conduire le courant en solution.
Hormis les matériaux supraconducteurs, les milieux, même conducteurs, ne conduisent pas
le courant de façon absolument idéale. Ils offrent une certaine résistance au passage du courant,
qui s'exprime en ohm, comme toute autre résistance électrique.
Plus la conduction du courant est satisfaisante, plus la résistance du milieu est faible.
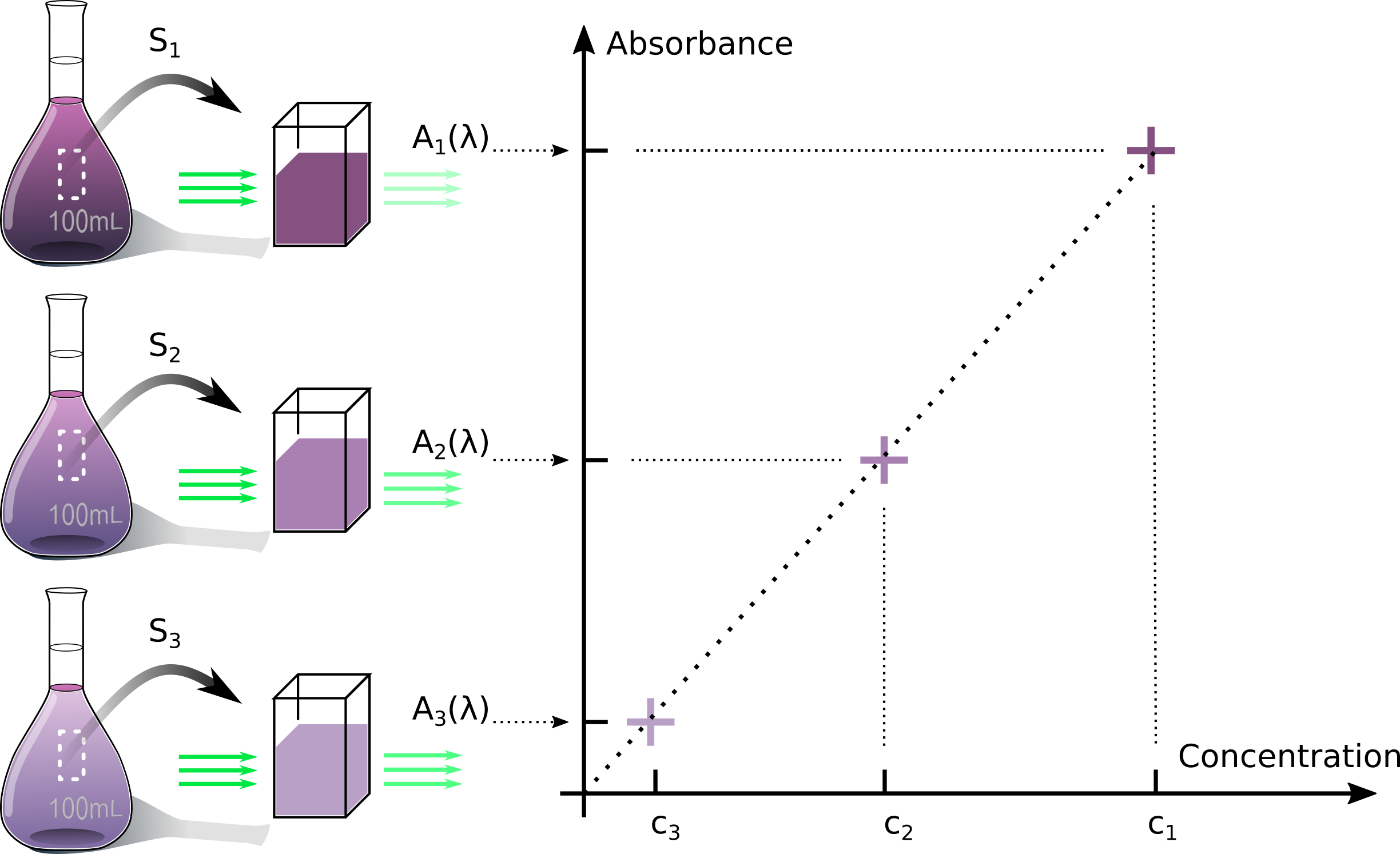
■ Un dosage par étalonnage est une technique expérimentale par comparaison.
Une gamme de solutions est préparée de façon bien connue au laboratoire. Ainsi, un même
soluté est dissous en quantités déterminées dans le solvant, produisant un éventail de
solutions aux concentrations bien connues. Ces solutions, qui s'apprêtent à servir de
références, sont appelées solutions étalons.
Par la suite, une même grandeur physique est mesurée dans chacune de ces solutions. Il
peut s'agir de l'absorbance, de la masse volumique, de l'indice de réfraction, etc.
Enfin, cette même grandeur est mesurée dans une dernière solution dont la concentration n'est pas
connue et est recherchée. En comparant la dernière mesure avec les précédentes, il est
possible de déterminer la valeur inconnue de la concentration recherchée.
■ Les gaz obéissent bien à la loi de Boyle-Mariotte, qui énonce que pour
une température donnée, et une quantité de gaz donnée, le produit de la
pression `p` du gaz et du volume `V` qu'il occupe est constant :
`p\cdotV=cste`.
Le produit d'une pression et d'un volume s'exprime en joules : cette loi est en
réalité une loi de conservation de l'énergie contenue dans le gaz, en lien avec son
énergie interne.