La composition du système chimique à chaque étape de la descente de burette est cette
fois-ci connue par la mesure de la conductivité du système.
La valeur de la conductivité est en effet changeante si la réaction support du titrage
consomme des ions, ou bien en apporte.
La courbe représentative `\sigma=f(V_{"burette"})` se scinde en deux domaines, modélisables
chacun à l'aide de droites. L'équivalence est repérée à l'intersection des deux droites
modélisant les deux domaines. On parle encore de rupture de pente.
 |
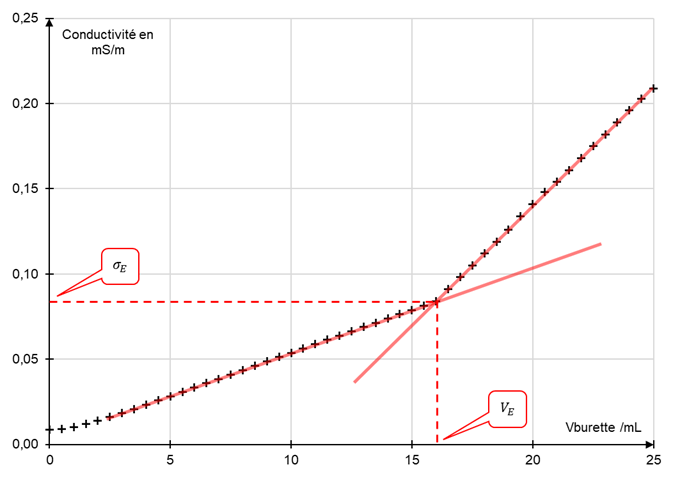 |
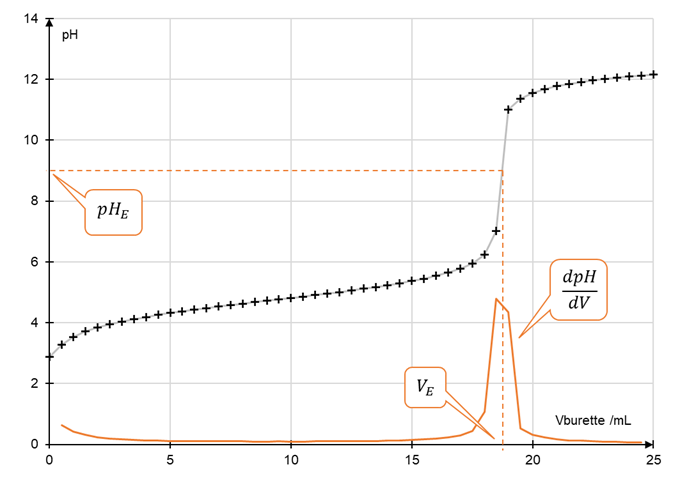
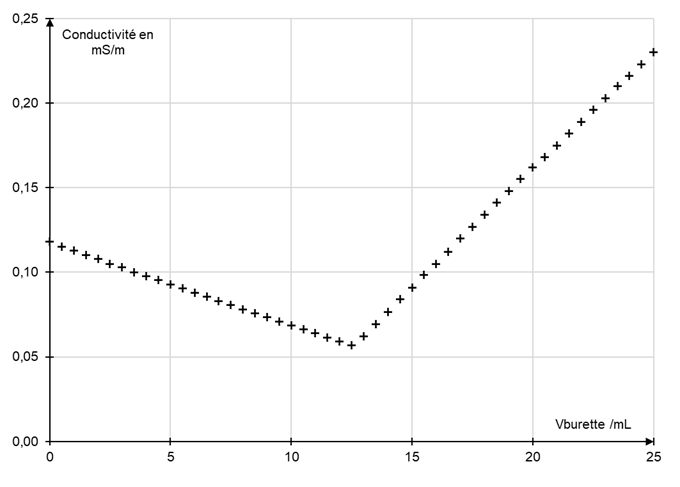
| Titrage de la soude par l'acide chlorhydrique
|
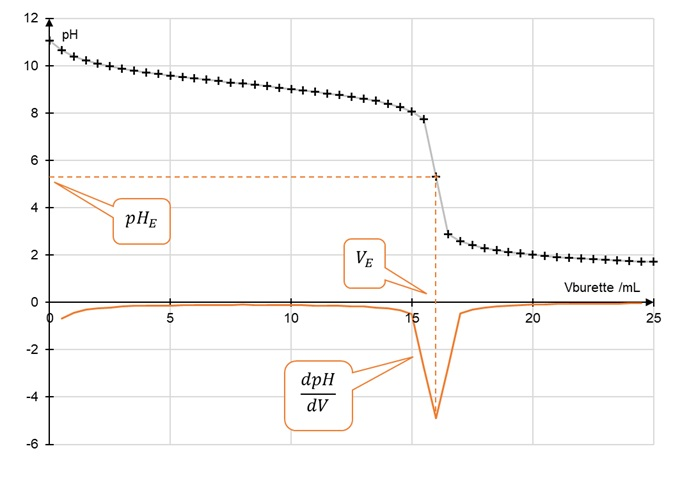
Titrage de l'ammoniac par l'acide chlorhydrique
|
Pour comprendre les sens d'évolution de la conductivité avant et après l'équivalence,
il faut mener un bilan exaustif de tous les ions présents dans le système, ou bien
consommés, ou bien ajoutés. Cela permet de comprendre si des ions, qui contribuaient
à la conductivité du système, ne sont plus présents ou bien inversement, si des ions
supplémentaires viennent à leur tour participer à la conduction du courant.
Exemple du titrage de la soude par l'acide chlorhydrique :
Le système contient initalement des ions sodium Na+ et hydroxyde HO-.
La burette contient des ions oxonium H3O+ et chlorure Cl-.
La réaction support du titrage est `HO^{-}(aq)+H_3O^+(aq)\to2\ H_2O(l)`.
■ Avant l'équivalence, comment évolue la contribution de chaque ion à la conductivité de la solution ?
- Des ions HO- sont consommés : leur contribution est perdue ;
- Des ions Na+ sont présents et spectateurs : leur contribution est maintenue ;
- Des ions H3O+ sont versés mais aussitôt consommés : aucune contribution ;
- Des ions Cl- sont ajoutés et spectateurs : leur contribution s'ajoute.
Ainsi, `\sigma` varie comme `(\lambda_{Cl^-}-\lambda_{HO^-})\cdot V_{"burette"}`.
Comme les ions chlorure, massifs, conduisent moins bien que les ions hydroxyde, la parenthèse
est négative, la pente est négative. La conductivité décroît avec la descente de burette.
■ Après l'équivalence, comment évolue la contribution de chaque ion à la conductivité de la solution ?
- Les ions HO- ont tous été consommés : plus aucune contribution ;
- Des ions Na+ sont présents et spectateurs : leur contribution est maintenue ;
- Des ions H3O+ sont versés sans être consommés : leur contribution s'ajoute ;
- Des ions Cl- sont ajoutés et spectateurs : leur contribution s'ajoute.
Ainsi, `\sigma` varie comme `(\lambda_{Cl^-}+\lambda_{H_3O^+})\cdot V_{"burette"}`.
La parenthèse est positive, la pente est positive, la conductivité croît lors de la descente de burette.
Remarque : la conductivité dépend de la concentration des ions (voir loi de Kohlrausch). Or la
descente de burette fait augmenter le volume du système, il y a un effet de dilution et donc
une baisse mécanique de la concentration des ions. Cet effet peut venir fausser l'étude qui doit
raisonner sur la consommation chimique des espèces présentes, ou leur production. Pour négliger
cet effet de dilution, il est d'usage d'ajouter au système un grand volume de solvant avant d'entamer
la descente de burette : ajouter 25 mL par la descente de burette, par rapport à un volume total
de 500 mL, ne représente qu'une variation de 5 %, ce qui rend bien l'effet de dilution négligeable.
Cet ajout d'eau n'a en revanche aucune incidence sur le volume équivalent car ajouter de l'eau ne
change pas la quantité d'espèce titrée qu'il faudra consommer à l'aide de l'espèce titrante.